科兴疫苗21天好还是28天好 科兴疫苗间隔21天好还是28天好
当地时间2021年5月3日,世卫组织公布了科兴生物灭活疫苗的评估报告:

目前的状态是:已经在45个国家或地区获批在18岁以上成人中使用,已经接种了2.6亿剂。

可供分析的数据:
一共有7个临床试验可供分析,在中国进行的是非劣效性试验,针对的是不同地区和老年人。

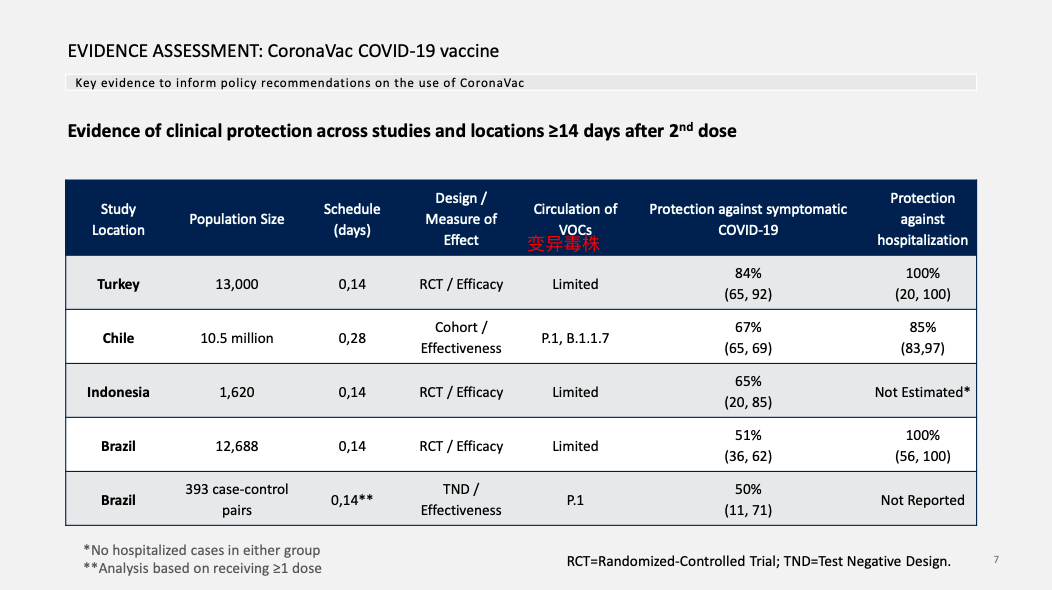
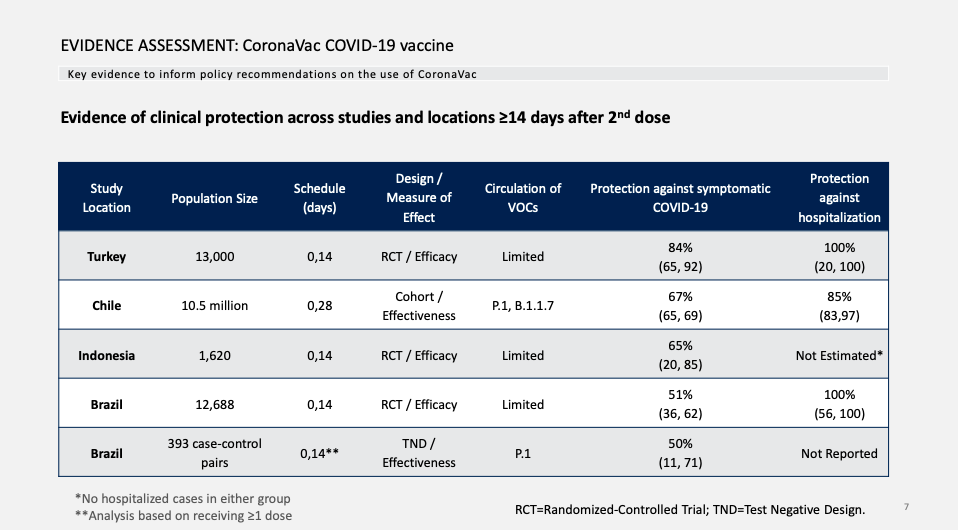
进行的临床试验概况
土耳其:无变异毒株(VOC),预防有症状的新冠肺炎效力84%,预防住院效力100%。
智力:巴西毒株(P.1)、英国毒株(B.1.1.7),预防有症状的新冠肺炎效力67%,预防住院效力85%。
印尼:预防有症状的新冠肺炎效力65%,对照组和疫苗组都没人住院。
巴西:随机试验,预防有症状的新冠肺炎效力51%,预防住院效力100%。看新闻:目前考虑数值较低的原因是间隔时间短(14天)、接种的是医务人员。(这一句不是who报告原内容)
巴西:配对病例对照试验:巴西毒株(P.1),预防有症状的新冠肺炎效力50%,预防住院效力数据未报道。
巴西的临床试验情况
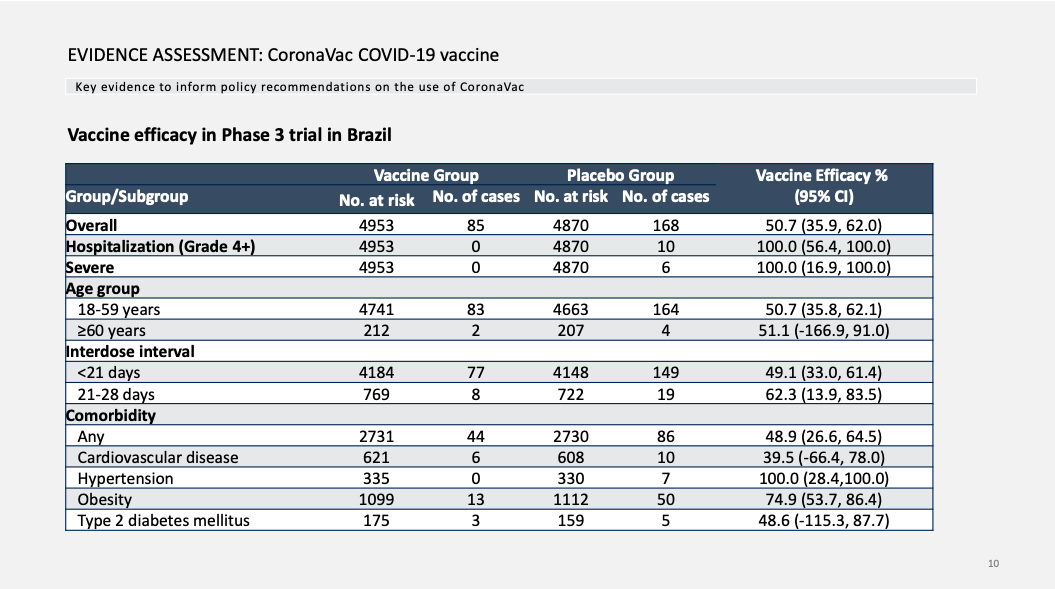
整体效力:50.7%,疫苗组85例感染,安慰剂组168例感染;
预防住院效力:100%,疫苗组0例住院,安慰剂组10例住院;
预防重症效力:100%,疫苗组0例,安慰剂组6例;
≥60岁以上的效力:51.1%,疫苗组2例,安慰剂组4例;
两针间隔时间在21-28天之间比<21天要高:62.3% vs 49.1%,所以接种间隔小于21天的,根据《新冠病毒疫苗接种技术指南(第一版)》,需要在2针后3周补打1针。
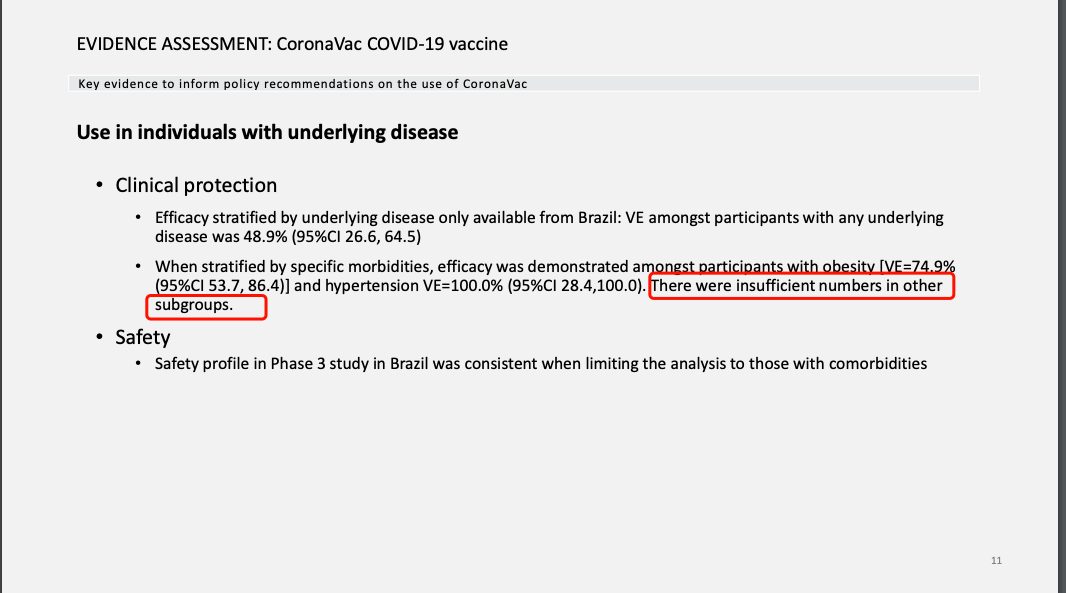
对于有合并症的志愿者:整体效力是48.9%,对合并高血压的志愿者效力最高为100%,对肥胖的志愿者效力是74.9,对合并心血管疾病的志愿者效力最低39.5%,对于合并2型糖尿病的志愿者效力次之48.6%,但是后两者数据不够,不能够作为结论。
安全性总结:
安全性良好,有两部分数据进行评估。
临床试验总结:
整体上安全,无严重不良事件,多是轻度/中度;
最常见的不良事件是注射部位疼痛、头痛、疲劳和肌痛。

授权后安全数据:
迄今为止没有发现监测以外的意外情况:
中国:根据分发的3580万剂和报告的49例严重不良事件,包括过敏反应、过敏性紫癜、喉水肿、脱髓鞘、脑出血(n≤6)
巴西/印度尼西亚:根据已分发的约1700万剂和报告的162例严重不良事件,包括发烧,呼吸困难、死亡、头痛(n≤16)
智利:根据分发的370万剂和报告的90次严重不良事件。最常见的是过敏反应的临床症状,报告率为1.7/100,000剂,低于另一种冠状病毒疫苗的报告率。

高龄人群数据
巴西是数据较低,但是在智利的4期试验证实了在老年人中的效力;
临床试验:与年轻人相比,安全性类似,但对老年人的反应原性较低;
授权后:大多数国家优先接种疫苗的年龄较大的年龄组,因此大多数报告往往是在这个年龄组。

智利临床试验结果:
预防有症状新冠肺炎效力67%,预防住院效力85%,预防进ICU效力89%,预防死亡效力80%。
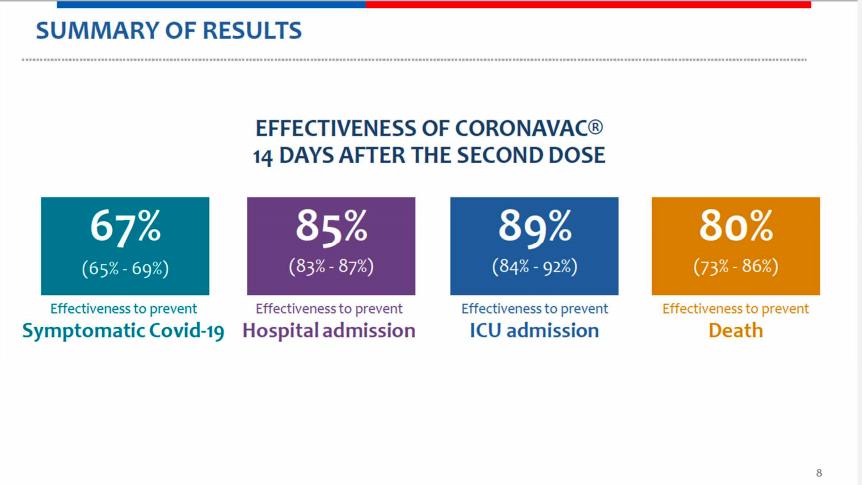
该临床试验就有足够的高龄人群:

证据等级
18-59岁人群的保护效力是非常确定的,高等级证据;但对于「严重不良事件风险较低」是中等证据,有一定信心认为发生严重不良事件风险较低;
60岁以上人群的保护效力有一定信心,是中等证据;对于「严重不良事件风险较低」证据等级较低;
有共病的人群的保护效力有一定信心,是中等证据;对于「严重不良事件风险较低」的证据等级较低。